
Fizikai Szemle nyitólap |
Tartalomjegyzék |
A Svéd Királyi Akadémia az 2994. évi kémiai Nobel-díjat George A. Olah, a University of Southern California, USA, professzorának ítélte a karbokation kémiához való hozzájárulásáért.
Karbokationok: hipotetikus közbülső termékektől a jóldefiniált molekulákig
Középiskolai kémiai tanulmányaink idejéről emlékszünk arra, hogy sok szervetlen vegyület, amilyen például a konyhasó, elektromos töltésű atomokból vagy atomcsoportokból épül fel. A konyhasó pozitív töltésű nátrium-ionok (Na+) és negatív töltésű klorid-ionok (Cl-) összekapcsolódásának tekinthető.1 Vegyünk egy másik példát: a “Glauber-só", Na2SO4, két Na+ ion és egy SO4--ion kapcsolódása.
Az ilyen elektromos töltésű részecskék - “ionok" gyakoriak a szervetlen vegyületek világában, ámde éppen ellenkező a helyzet a szerves vegyületek, különösen szénhidrogének esetén. A szénhidrogének két elemből álló vegyületek: hidrogénhól (H) és szénből (C) állnak. A szénhidrogének a szerves vegyületek igen nagy és fontos csoportját alkotják - például a legtöbb természetes ásványolaj-termék szénhidrogén. Jóllehet a századforduló táján néhány kémikus előállított olyan szénhidrogéneket, amelyekről azt gondolták, hogy ionosak - például a benzolból és a metánból készített egyik vegyületcsoportról (a triarilmetán származékokról) -, de ezeket általában kuriózumoknak tartották.
Amikor néhány angol (Ingold és Hughes) és német (Meerwein) vegyész az 1920-as és 1930-as években azt kezdte tanulmányozni, hogyan zajlanak le a kémiai reakciók a szerves molekulák között, világossá vált, hogy előfordulhatnak pozitív töltésű szénhidrogének - melyeket a vegyészek “karbokationoknak" neveznek - nagyon rövidéletű (mikro- vagy nanoszekundumos élettartamú) közbülső termékekként.
Mivel a posztulált “karbokation intermediérek" valószínűleg nemcsak nagyon rövid élettartamúak, hanem nagyon reakcióképesek is, föltételezték, hogy sohasem tudják majd megfelelő mennyiségben előállítani őket. Tulajdonságaikat sem lesznek képesek tanulmányozni olyan fizikai módszerekkel - például NMR vagy infravörös (IR) spektroszkópia és röntgendiffrakció segítségével -, mint amilyenekkel a normális, töltéssel nem rendelkező szénhidrogéneket vizsgálják. Ám a kutatás iránya tökéletesen megváltozott az ezévi kémiai Nobel-díjas, George A. Olah professzor eredeti és nagy képzelőerőről tanúskodó munkája nyomán.
Az 1960-as évek elején Olah és munkatársai felfedezték, hogy elő lehet állítani stabil karbokationokat egy új típusú, különösen savas vegyületek felhasználásával amely sokkal erősebbek, mint az olyan klasszikus savak, mint a kénsav, a sósav stb. Ezek az új savak - amelyek közül néhányat a kanadai szervetlen kémikus, R.J. Gillespie írt le először - “szupersavakként" váltak ismertté. Előállítható szupersav például hidrogén-fluoridból (HF) és antimon-pentafluoridból (SbF5).
Olah felfedezése alapvetően átalakította a tünékeny karbokationok kutatását. Az eredeti felfedezés óta igen sok karbokationt állítottak elő, tulajdonságaikat részletesen tanulmányozták. Olah azt is megmutatta, hogyan lehet a szupersavakra és karbokationokra vonatkozó alapkutatást új és fontos szerves vegyületek egyszerű szintézisére alkalmazni, és azt is, hogy számos kis szerves molekulát - melyeket kiinduló anyagként széleskörben használnak a nagyszabású szintéziseknél - lehet előállítani egyszerű és olcsó módszerrel, ha szupersavakat alkalmaznak katalizátorként. Munkája eredményeként új módszerekkel lehet átalakítani az egyenes szénláncú szénhidrogéneket (ezeknek kicsi az oktánszámuk a robbanómotorokban és nehéz biológiailag lebontani őket) olyan elágazó szénhidrogénekké, amelyeknek magas az oktánszáma és biológiailag könnyen lebonthatóak.
Olah tudományos teljesítményét széles körben elismerik a szerves kémikusok, karbokationokra vonatkozó munkái előkelő helyen szerepelnek a modern szerves kémiai tankönyvekben.
Kutatási eredmények
George A. Olah a szénvegyületekből képzett, szupersavas oldószerekben és alacsony hőmérsékleten lévő kationokra (karbokationokra) vonatkozó kutatásaival új utat nyitott ezek szerkezetének és reakcióképességének részletes megismerése. számára. Munkája olyan új, reakciók felfedezéséhez vezetett, melyeknek nagy jelejtőségük van a vegyiparban és másutt.
A kémiai reakciókban az eredeti anyag molekulái végtermékké alakulnak át. Ez leggyakrabban rövidéletű (10-10 - 10-6 másodperc), nagy reakcióképességű köz-, benső anyagokon keresztül történik. Sok szerves kémiai reakció közbenső termékei karbokationok. Mivel ezek nagyon rövid élettartamúak, olyan alacsony koncentrációban fordulnak csak elő, hogy nem lehet őket közvetlenül megfigyelni például spektroszkópiával. A létezésükre, szerkezetükre, reaktivitásukra stb. vonatkozó ismeretek ezért sokáig nagyon hiányosak voltak.
Fontos megérteni, hogyan zajlanak le a reakciók ahhoz, hogy irányítani tudjuk tudjuk őket, és úgy avatkozzunk a folyamatokba, hogy a kívánt termékekhez jussunk. Kiváltképp fontos ez a vegyiparban. Olah arra törekedett, hogy a rövidéletű karbokationoknak hosszú életet adjon. El kellett érnie, hogy lassabban reagáljanak az oldószerekkel és más nukleofil molekulákkal. (Nukleofilok azok az anionok vagy oldószerek melyeknek szabad elektronpórjuk van, és amelyek meg tudják támadni a molekulában lévő pozitív ionokat vagy pozitív módon polarizált atomot.) Olah olyan oldószereket használt, amelyek nagyon kevéssé nukleofilok (például SO2, SO2ClF és SO2F2), ezért alacsony hőmérsékleten lassan reagálnak a karbokationokkal. A karbokationok elállításához viszont szupersavakat használt (olyan savakat, amelyek erősebbek mint a 100 %-os kénsav).
Alkilhalogenideket oldott fel alacsony hőmérsékleten hidrogén-fluorid-antimon-pentafluoridban (HF-SbF5, mely 1018-szor erősebb, mint a 100 %-os kénsav. Ezzel három vegyértékű karbokationokat (karbenium-ionokat) olyan nagy koncentrációban és olyan hosszú élettartammal sikerült előállítania, hogy mágneses magrezonancia spektroszkópiával (NMR) és elektronspektroszkópiával (ESCA) tanulmányozni tudta szerkezetüket, stabilitásukat, tulajdonságaikat és reakcióképességüket. Olah úttörő munkája lehetővé tette, hogy különböző spektroszkópiai módszerekkel közvetlenül megfigyeljék a karbokationokat, így részletesen megismerjék szerkezetüket és reaktivitásukat.
Olah azt is felfedezte, hogy a szupersavak olyan erősek, hogy az egyszerű szénhidrogénekhez több hidrogén-iont is tudnak kötni, és így pentakoordinált karbokationok (carbonium-ionok) képződnek. Ennek már gyakorlati következménye is volt a szénhidrogén-kémiában, mert például új módszerekhez vezetett a szénhidrogének izomerizációjára és a magasabb szénatom-számú szénhidrogének metánból való szintézisére vonatkozóan.
Sokféle szerkezetű és nagy számú karbokationt tanulmányoztak mostanáig. A kutatások sok meglepő és fontos eredményt hoztak a kémiai kötés megértésével kapcsolatban. A három vegyértékű (tűkoordinált) karbokationokon kívül a magasabb koordinációjúakat - tetra-, penta- és hexakoordinációjúakat - is előállították és tanulmányozták a szerkezetüket. Leomlott a szénatom négyvegyértékűségére vonatkozó régi dogma, amely Kekulé óta, azaz az 1860-as évek óta a szerkezeti szerves kémia alaptétele volt.
Történet
Az 1920-as években, főként C.K. Ingold (1893-1970) kutatásai nyomán sok szerves kémiai reakció mechanizmusát feltárták. A szintetikus szerves kémiában alkalmazott két legközönségesebb és legszélesebb körben felhasznált reakció a nukleofil szubsztitúció és az elimináció. A nukleofil szubsztitúció során a reagens (a nukleofil) elektronpárt visz át a szubsztrátumra, amely ezt az elektronpárt használja fel az új kötés kialakítására, míg az eltávozó csoportról kilép egy elektronpór. Az eliminációs reakciókban a szomszédos szénatomokon lévő két csoport kilép és olefin (alkil) keletkezik. A szubsztrátum szerkezetétől, az oldószertől és egy sor más tényezőtől függően, ezek a reakciók két fázisban mennek végbe. Ezeket példázza az izopropil-klorid, amely egy nukleofil (Nu-) jelenlétében nukleofil szubsztituciós és/vagy eliminációs terméket ad:
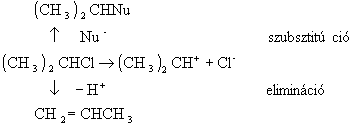
Az első fázisban a szén-klór kötés felbomlik, és rövidéletű karbenium-ion keletkezik. A következő lépésben ez gyorsan reagál vagy a Nu--val és szubsztituciós termék keletkezik, vagy átvisz egy protont az oldószerre vagy a Nu--ra és propént kapunk. A kiterjedt kinetikai
és sztereokémiai vizsgálatok konzisztensnek mutatkoztak az olyan mechanizmusokkal, amelyek karbokation intermediéreket foglalnak magukban. Föltételezett átmeneti termékekként karbenium-ion-struktúrákat és karbonium-ion-struktúrákat (nem-klasszikus ionok) javasoltak. Az eredmények magyarázatához azt is fel kellett tételezni, hogy a karbokationok gyakran egyesülhetnek bizonyos negatív töltésű ionokkal, így kontakt-ionpórokat vagy oldószer-elválasztott ionpórokat adnak. Ez utóbbi kutatás főként S. Winstein (1912 - 1969, USA) nevéhez kapcsolódik.
A vizsgált karbokationok azonban olyan rövid élettartamúak voltak (10-10 - 10-6 másodperc), hogy spektroszkópiailag nem lehetett őket közvetlenül megfigyelni. Ezekről a fontos intermedierekről még mindig nem teljes a képünk.
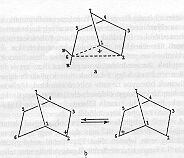 1. ábra. Karbenium-ion (a), egyensúlyban lévő karbenium-ion (b) |
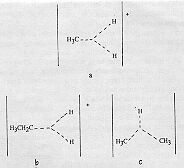 2. ábra. |
Olah különlegesen fontos hozzájárulása ezekhez a kutatásokhoz az általa kifejlesztett módszerben rejlik, amely segítségével nagy koncentrációjú karbokationokat állított elő olyan feltételek között, amelyek számukra hosszú élettartamot biztosítottak. Ezt úgy érte el, hogy olyan különlegesen kevéssé nukleofil oldószereket használt, amelyek nem támadták meg a karbokationokat. Ilyen oldószerek. a SO2, az SO2ClF és SO2F2, Ezekben, legalábbis -100 °C körüli hőmérsékleten, a karbokationok élettartama hosszú. A karbokationok előállításához Olah különféle szupersavakat használt, köztük SbF5 öt, mely Lewis-szupersav és alkilhalogenidekkel karbokationokat ad. A többi Bronsted-szupersav, például HSO3F vagy azok a különlegesen erős szupersavak, amelyeket például HSO3F vagy HF és SbFS kombinálásával lehet nyerni. A Mágikus Sav®, a HSO3F:SbF5 és a HF:SbF5, 1018 -szor erősebb, mint a 100 %-os kénsav. Ezek közül a Mágikus Sav® és a HF:SbF5 olyan erősek, hogy az alkoholokat és olefineket teljesen protonálni tudják, és nagy koncentrációban keletkeznek karbokationok. Általában -78 °C - -120 °C hőmérsékletet alkalmaznak. Különösen a 1H és 13C NMR-vizsgálatok adtak részletes ismereteket a karbokationok szerkezetéről, stabilitásáról és reaktivitásáról.
A nukleofil szubsztitúcióra és a 2-norbornil származékokra vonatkozó vizsgálatok az 1950-es években vezették S. Winsteint arra a feltételezésre, hogy az intermediér karbokation nem-klasszikus és pentakoordinált szénatomot tartalmaz (C az 1.a ábrán két hidrogénhez koordinálódik a C1, C2 és C5-ön kívül). Ezt az értelmezést megkérdőjelezte H.C. Brown (1912, USA), aki az 1979. évi kémiai Nobel-díjat azért kapta, mert a bórvegyületeket fontos reagensként alkalmazta szerves szintézisekben. Brown szerint a 2-norbornil kationnak nincs karboniumion szerkezete, hanem ez karbenium-ion, amely gyorsan visszaalakul önmagába, vagyis ez egy gyorsan egyensúlyba kerülő karbenium-ion (1.b ábra).
A tudományos vita körülbelül 1980-ig tartott. Mivel a karboniam-ionok struktúrája elméletileg igen fontos volt, a probléma sok vezető fizikai szerves kémikust ragadott magával, ámde a nagy erőfeszítések és leleményes kísérletek ellenére határozott megoldást nem találtak egészen addig, amíg a 2-norbornil kationt nem tudták NMR spektroszkópiával tanulmányozni.
Olah és munkatársai végül megfigyelték a 2-norbornil karbokationt SbF5 - SO2ClF-SO2F2 oldatban -158 °C-on. Ezen az alacsony hőmérsékleten mind a 1,2 hidrid eltolódások, mind pedig a bonyolultabb visszarendeződések elegendően lassúak ahhoz, hogy ne zavarják az NMR spektrumok értelmezését.
A spektrumok teljes összhangban álltak Winstein szimmetrikus hídszerkezetével, a pentakoordinált szén-atomokkal (1.a ábra) és nem álltak összhangban a gyorsan egyensúlyba kerülő karbenium-ion feltevésével. A kémiai analízisre használt elektronspektroszkópia (ESCA), melyet az 1981-es fizikai Nobel-díj kitüntetettje, a svéd Kai Siegbahn fejlesztett ki, megerősítette ezeket a következtetéseket.
A pentakoordinált szénatomokat tartalmazó molekulák többé nem tekinthetők a szerves kémia egzotikus kuriózumainak. Megtalálták őket szervetlen vegyületekben, fémorganikus vegyületekben, például organolítium vegyületekben, karboránokban és más klaszter vegyületekben is.
A szupersavak olyan erősek, hogy képesek protonálni olyan különlegesen gyenge bázisokat is, mint az alkánok, ahogy Olah és tőle függetlenül H. Hogeveen kimutatta. Ily módon a metánnál magasabb szénatomszámú alkánokból és különböző cikloalkánokból pentakoordinált karbonium-ionokat kaptak. A metán metionium-iont (CH5+) ad, amelyet Olah úgy írt le, hogy három centrumú kételektronos kötést tartalmaz (2.a ábra, háromszögalakú szaggatott vonal). Megjegyzendő, hogy a vonalelágazás nem jelent újabb atomot. A magasabb alkánok mind a C-H kötésnél (2.b ábra), mind pedig a C-C kötésnél protonálhatók (2.c ábra).
Olah azt találta például, hogy a protonáll izobután t-butil kationra és molekuláris hidrogénre bomlik. Klasszikus szemmel nézve ez teljesen értelmetlen reakció; az izobutánt a proton oxidálja, és t-butil kation és molekuláris hidrogén keletkezik.
(CH3)3CH+ ![]() (CH3)3C+ + H2
(CH3)3C+ + H2
A telített szénhidrogének protonáfása szupersavakban, Olah munkássága nyomán, már gyakorlati következményekhez is vezetett. Elvezetett egy olyan módszerhez, amellyel az egyenes szénláncú alkánokat magasabb oktárszámú elágazó szénláncú alkánokká lehet izomerizálni. Lehetővé tette, hogy metán-egységekből magasabb szénatomszámú alkánokat állítsanak elő, például metánból etánt. A szupersav-katalízis révén meglepően enyhe körülmények között tudták a nehéz olajokat krakkolni, a szenet pedig cseppfolyósítani.
2 CH4  CH3CH3
CH3CH3
Olah újabban kimutatta, hogy a legközönségesebb elektrofiljeink, amilyen például az acil-kation és a nitróniumion, szupersavas közegben duplatöltésű szuperelektrofilekké protonálódnak. Ez az elektrofil reakcióképesség drámai növekedéséhez vezet. Már most is nyilvánvaló, hogy Olah új kémiájának igen széleskörű és fontos alkalmazásai vannak.
Oláh György
Oláh György 1927. május 22-én született Budapesten. [Miként a másik magyar kémiai Nobel-díjas, Hevesy György, ő is a Piarista Gimnáziumba járt.] A budapesti Műszaki Egyetemen szerzett vegyészmérnöki oklevelet és 1949-ben ott doktorált. A Budapesti Műszaki Egyetemen különböző állásokat töltött be 1949 és 1954 között. A Szerves Kémiai Tanszék vezetője volt. [1954-ben, 27 évesen lett a kémiai tudományok doktora. A flourvegyületek kémiáját kutatta.] Ezután az MTA Központi Kémiai Kutató Intézet igazgatóhelyettese volt 1954-től 1956-ig. Olah 1957-ben települt Észak-Amerikába. A Dow Chemical Company tudományos főmunkatársa lett Kanadában, majd az USA-bar 1957-től 1964-ig. 1965-1977-ig a Case Western Reserve University professzora volt, 1977-ben kinevezték a University of Southern California Szénhidrogénkutató Intézetének tudományos igazgatójává. 1991-ben a Loker Szénhidrogénkutató Intézet igazgatója lett. George A. Olah amerikai állampolgár. Címe: Locker Hydrocarbon Research Institute, University of Southern California, Los Angeles, CA 90089, USA.
_____________________________
1 A Svéd Királyi Akadémia sajtótájékoztatója. (Fordította Palló Gábor)